
Accueil
Comité d’éthique de la SFCR
Les lois encadrant la recherche clinique impliquant la personne humaine ont été modifiées en Novembre 2016 par la loi Jardé dont les décrets d’application ont été publiés dans les mois qui suivent. Elles imposent d’obtenir un avis favorable d’un Comité de Protection des Personnes (CPP) pour toute étude prospective, qu’elle soit interventionnelle ou observationnelle. Depuis l’arrêté d’avril 2018 définissant les catégories RIPH3, il n’y a plus que les études rétrospectives, les études d’évaluation de satisfaction et les évaluations pédagogiques qui ne sont pas soumises à un accord du CPP.
Or, toute recherche est destinée à être publiée et la plupart des revues internationales dont la revue « Neurochirurgie » exigent l’avis d’un Comité d’Ethique de la Recherche (Institutional Review Board (IRB) des anglo-saxons), en référence à la déclaration d’Helsinki, avec communication du numéro d’enregistrement de l’avis et parfois du courrier le communiquant.
La SFCR a donc créé son IRB enregistré auprès autorités Américaines (Office for Human Research Protections ; U.S. Department of Health and Human Services ) référencé sous le numéro : IRB00014665
La SFCR est enregistrée auprès de l’ Office for Human Research Protections sous le numéro : IORG0012392
Mission de l’IRB
• Statuer sur le caractère non interventionnel d’un projet de recherche clinique qui lui aura été soumis pour avis en vue d’une publication,
• Emettre tout avis éthique entrant dans le champ de la neurochirurgie
• S’assurer du caractère éthique de tout projet de recherche fondé sur l’utilisation des bases de données de la neurochirurgie
• L’avis ne vaut pas autorisation de recherche que seul le promoteur de l’étude peut donner, l’avis n’a pas de valeur juridique mais uniquement éthique.
Membres
L’IRB est constitué de 5 membres :
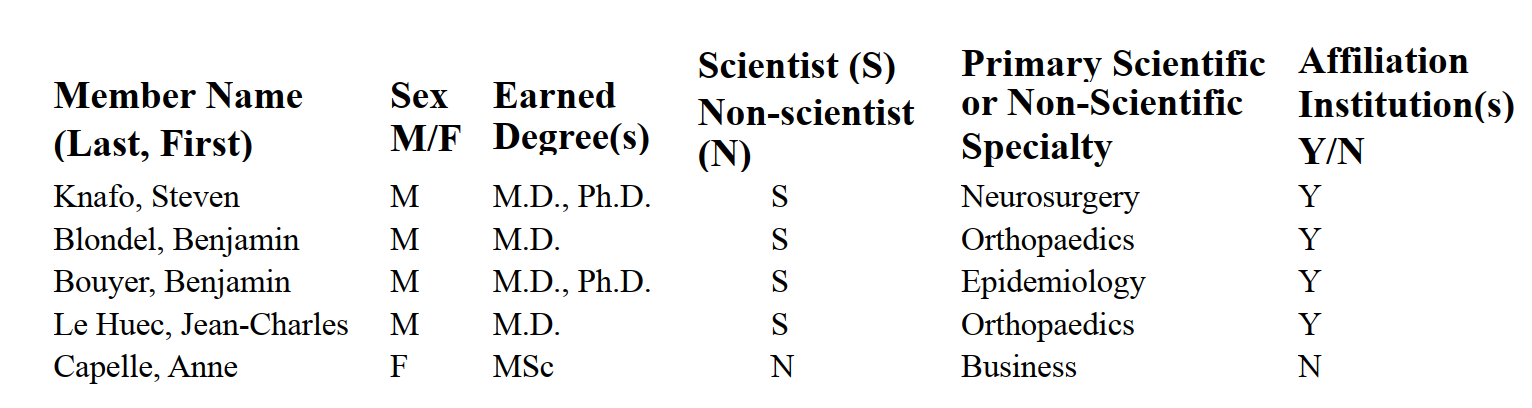
Fonctionnement
Le fonctionnement de l’IRB est dématérialisé via le site de la SFCR sur laquelle les soumissions de projets sont faites par les investigateurs et les avis rendus par les experts (à l’exclusion de tout autre moyen de soumission).
Les soumissions doivent comporter un résumé de moins de 500 mots et préciser : le nom de l’investigateur principal, le ou les lieu(s) de l’étude, s’il s’agit d’un projet ou d’une étude déjà réalisée, le type d’étude (prospective, rétrospective…), si une information a été donnée aux patients et si oui sous quelle forme (document d’information, consentement…) et quelles informations ont été données.
L’IRB donne une réponse dans les deux mois.
Trois types d’avis sont rendus :
- 1) Avis favorable
- 2) Relève d’un CPP
- 3) Avis défavorable pour raison éthique
Seul l’avis favorable conduira à la numérotation de l’avis type : Avis favorable n° IRB00014665_SFCR_IRB #1_2025/1
L’avis favorable nécessite l’unanimité des membres éventuellement après discussion des membres
L’avis final comportera :
- Le numéro d’ordre de l’avis
- L’identification et l’intitulé de la recherche ;
- Le nom de l’investigateur ou, le cas échéant, de l’investigateur coordonnateur ;
- Le nom du promoteur (s’il y a lieu) ;
- Le lieu où se déroule la recherche, lorsqu’il est soumis à autorisation ;
- La date à laquelle l’avis a été rendu
- L’avis et sa motivation.
- Cet avis final est rédigé en français ou en anglais si la soumission est en anglais.
Un rapport annuel de fonctionnement de l’IRB sera exposé au congrès annuel et mis en ligne sur le site de la SFCR.
* pages adaptées du Collège de Neurochirurgie
